8月24日,科济药业(股票代码:2171.HK)公布2022中期业绩。
业绩亮点速览
- CT053完成中国关键II期临床试验入组,计划于2022年第三季度在国内提交NDA
- CT041被FDA授予“再生医学先进疗法”(RMAT)
- CT041中国研究者发起试验的数据在《Nature Medicine》发表
- 持续开发创新CAR-T技术,布局下一代管线候选产品
- 美国CGMP生产工厂启动运营,于下半年支持北美临床试验
- 委任科济药业首席医学官及旗下美国公司总裁,加强领导团队力量
科济药业董事长、首席执行官、首席科学官李宗海博士表示:回顾2022年上半年,虽然疫情带来了一些挑战,但科济药业在管线产品的临床开发、技术创新及在中国和美国的业务运营方面,均取得了重大的进展。目前,CT041已成为全球首个且唯一进入确证性II期临床试验的实体瘤CAR-T产品,CT053即将于第三季度在国内提交NDA申请。公司位于美国的CGMP生产工厂也启动运营。我们持续推进CAR-T技术创新以攻克行业重大挑战,同时我们也建立了独立自主、垂直一体化的生产能力。我们将始终秉承“科创济世”的愿景,早日为全球癌症患者带来创新和差异化的细胞疗法,也为广大投资者和社会公众创造更多价值。
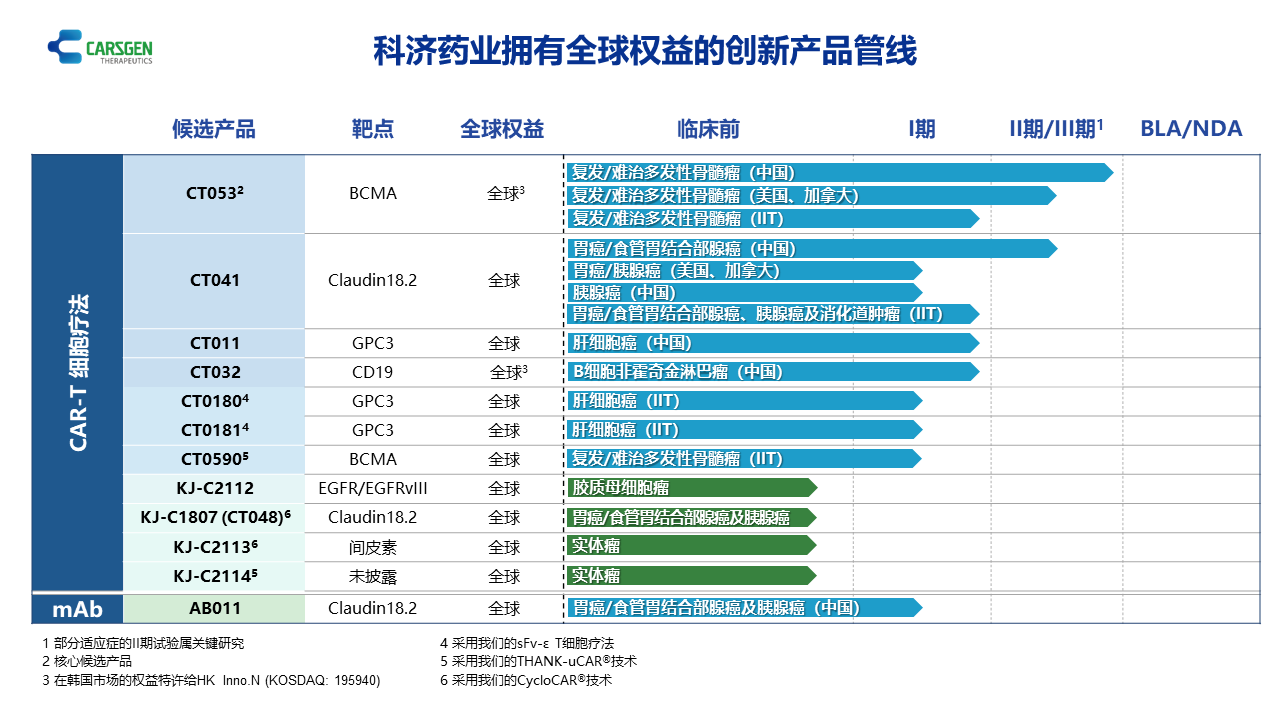
产品管线稳步推进,实体瘤CAR-T保持领先
CT053是一种升级的、用于治疗复发/难治多发性骨髓瘤(R/R MM)的全人抗BCMA自体CAR-T细胞候选产品。其融合了具有较低免疫原性和较高稳定性的全人抗BCMA特异性单链抗体的CAR结构,在没有肿瘤相关靶点的情况下,可降低CAR-T细胞的自动激活,克服了T细胞耗竭的问题。CT053就治疗R/R MM于2019年获得美国FDA的再生医学先进疗法(RMAT)及孤儿药认定,以及就治疗R/R MM于2019年获得欧洲药品管理局(EMA)的优先药物(PRIME)资格及于2020年获得孤儿药产品认定,并就治疗R/R MM于2020年获得国家药监局的突破性疗法认定。科济已经完成中国关键性II期试验(LUMMICAR STUDY 1)的患者入组,并计划于2022年第三季度向国家药监局提交新药上市申请(NDA)。科济正在北美进行关键性2期试验(LUMMICAR STUDY 2),并计划于2023年向美国FDA提交生物药物上市许可申请(BLA)。公司亦计划进行额外临床试验,以开发CT053作为多发性骨髓瘤的早期治疗方法。CT053中国研究者发起的试验(IIT)研究结果于2022年在《Haematologica》杂志发表。CT041是一种全球潜在同类首创的,靶向Claudin18.2(CLDN18.2)蛋白的自体CAR-T细胞候选产品。CT041用于治疗CLDN18.2阳性实体瘤,主要治疗胃癌/食管胃结合部癌(GC/GEJ)及胰腺癌(PC)。科济在全球范围内率先成功识别、验证并报告CLDN18.2可作为实体瘤的相关抗原,是治疗CLDN18.2普遍及高表达的实体瘤CAR-T细胞疗法的可行靶点。CT041就治疗GC/GEJ于2020年取得美国FDA的孤儿药认定以及就治疗晚期胃癌于2021年取得EMA的孤儿药产品认定。CT041就治疗晚期胃癌于2021年获EMA授予PRIME资格,及就治疗CLDN18.2阳性晚期GC/GEJ于2022年获得RMAT认定。截至公告日,CT041是全球首个且唯一进入到确证性II期临床试验的用于治疗实体瘤的CAR-T细胞候选产品。科济正在进行的试验包括在北美的一项针对晚期GC/GEJ和PC的1b/2期临床试验(CT041-ST-02,NCT04404595),在中国的一项针对晚期GC/GEJ和PC的Ib期临床试验和一项针对晚期GC/GEJ的确证性II期临床试验(CT041-ST-01,NCT04581473)以及IIT。科济计划于2024年上半年向中国国家药监局提交NDA。CT041在美国现已完成剂量爬坡并已启动剂量扩展。科济亦计划于2022年下半年在北美启动一项2期临床试验,并于2024年向美国FDA提交BLA。CT041在美国的1b期研究(NCT04404595)的结果及在中国的Ib/II期研究(NCT04581473)的结果于2022年6月举行的2022年美国临床肿瘤学会(ASCO)年会上以壁报形式进行展示。中国研究者发起的试验的结果于2022年5月在《Nature Medicine》发表,是首个发表于顶级学术期刊的迄今为止最大样本量的CAR-T细胞治疗实体瘤临床研究。AB011是一种靶向CLDN18.2的人源化单克隆抗体候选产品,用于治疗CLDN18.2阳性实体瘤。科济就靶向CLDN18.2的单克隆抗体取得该靶点全球第二项试验用新药(IND)许可。科济正在中国进行AB011用于治疗CLDN18.2阳性实体瘤的I期临床试验,现已完成I期单药入组并启动联合化疗阶段试验。科济已建立了涵盖整个CAR-T开发周期的综合研发平台,包括靶点发现、抗体开发、载体设计、制造、质量保证以及质量控制。科济持续投身于推进CAR-T技术创新,以攻克行业重大挑战。公司的四大战略支柱包括:(1)疗效:为提升治疗实体瘤的疗效,科济持续开发下一代CAR-T技术,如CycloCAR®。CycloCAR®的特色是在CAR-T细胞中共同表达细胞因子IL-7和趋化因子CCL21,有望产生更高的临床疗效并减少清淋化疗预处理。(2)安全性:为提高过继性细胞疗法的适用性,科济开发了基于sFv-ε的T细胞疗法,其由GPC3靶向的scFv和CD3ε亚单位组成的全T细胞受体(TCR)复合物提供动力,可与其他TCR亚单位形成功能性TCR复合物,重定向T细胞以非MHC依赖性方式杀伤肿瘤细胞。(3)患者可及性:科济正在开发使用THANK-uCAR®技术的同种异体CAR-T细胞候选产品。公司认为该技术有望促进CAR-T细胞的增殖、持久性及疗效。公司相信,成功应用THANK-uCAR®技术将大幅降低CAR-T细胞疗法的成本,提高患者可及性。(4)靶点可用性:科济开发了LADAR®技术(由人工受体驱动的局部作用),其中人工受体由LADAR®配体触发,诱导目标基因的转录。通过LADAR®人工受体,只有当LADAR®与LADAR®配体结合时,才会触发抗肿瘤CAR转录,从而可以精准控制免疫细胞何时及于何种情况下作用于癌细胞。目前上述技术均为自主研发,拥有全球权益,可单独或结合使用以升级科济的现有候选产品及产生未来的管线候选产品。截至2022年6月30日,科济拥有超过300项专利,其中有70项为全球(包括中国、美国、欧洲及日本)授权专利。相较2021年底,增加了7项授权专利及21项专利申请。科济已建立了自主、垂直一体化的生产能力,包括质粒生产、慢病毒载体生产和CAR-T细胞生产。公司持续扩大在中国和美国的全球产能,以支持临床试验和随后的管线产品的商业化。利用公司在上海徐汇区的临床生产工厂以及位于上海金山区的商业GMP生产工厂,公司能够独立自主地生产CAR-T细胞以支持在中国的临床试验,以及独立自主地生产慢病毒载体以支持全球的临床试验。今年,公司通过启动位于美国北卡罗来纳州达勒姆三角研究园(RTP)的CGMP生产工厂,于扩大公司在中国以外的产能方面取得重大进展。工厂顺利通过了官方检查,并已获得达勒姆市县检验局颁发的合规证书,并经与FDA进行RMAT协商后启动RTP生产工厂的调试、资质及验证工作。同时,科济一直在执行向RTP生产工厂的技术转让,推进CT041及CT053产品的临床生产。截至2022年6月30日,科济共有601名雇员。公司亦加强了领导团队的力量:聘请Raffaele Baffa博士担任科济药业首席医学官及Richard Daly先生担任CARsgen Therapeutics Corporation(科济药业旗下美国公司)总裁。高级管理人员履历详情载于公司网站(www.CARsgen.com)。科济药业(股票代码:2171.HK)是一家在中国及美国拥有业务的生物制药公司,主要专注于治疗血液恶性肿瘤和实体瘤的创新CAR-T细胞疗法。我们建立了一个综合细胞治疗平台,其内部能力涵盖从靶点发现、抗体开发、临床试验到商业规模生产。我们通过自主研发新技术以及拥有全球权益的产品管线,以解决CAR-T细胞疗法的重大挑战,比如提高安全性,提高治疗实体瘤的疗效和降低治疗成本。我们的使命是成为能为全球癌症患者带来创新和差异化的细胞疗法,并使癌症可治愈的全球生物制药领导者。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!