2022-09-28 14:34:45Source:博药/红辣椒Views:290
导读:中国仿制药将往何处?
仿制药是指在剂型、安全性、规格、给药途径、质量、性能特征和预期用途等方面与已上市的原研药相同的药物。任何仿制药在剂量、剂型、给药途径、安全性、有效性、药力、标签等方面必须与原研药品相同(某些有限的例外)。它必须达到与原研产品同样高的质量和制造标准,质量、使用和使用方法也必须相同。但虽说如此相似,仿制药终归比不上原研药,就像六耳猕猴终究比不上齐天大圣。
仿制药VS原研药
价格“扶伤”
仿制药与原研药差异的根源来自开发模式的不同。原研药需要经过漫长的研发周期(10-15年)、高额的研发费用(接近20亿美元)、超高的失败率(90%),可谓百炼成金。而仿制药就不一样了,它只需要证明自己是原研药的“影子”,与之对应的就是大大缩短的研发周期(2-4年)、低廉的研发成本(创新药的1%)。
从开发模式走向的终点来看,横亘在原研药和仿制药之间的从来就不是技术问题,而是专利。1984年,美国《Hatch—Waxman法案》规定原研药的专利期限延长为20年,从临床试验前开始申请的话,等到新药获批上市时间其实已经过去大半,剩下的有限时间里,新药承担着回收成本加创收的重任,价格自然低不了。
所以,尽管市面上出现了如紫微星降世的救命药,但高昂的价格对普通人而言,依旧可望而不可即。本来是个大喜事儿,但是最终的结果并不能让大家满意。降价?开放专利?不可能的,救死扶伤的基础建立在经济之上,现在也还没实现共产主义社会。美国著名经济学家曼斯菲尔德的一项研究指出,如果没有专利保护,60%的新药不会被发明出来。
一方面是驱动社会进步的创新,另一方面是亟待解救的人民。手心手背都是肉,但总有取舍在,而这个折中点就是仿制药。哪儿都有穷人,原研药的贵刺痛了每个国家。也因此,获得绝大部分民众负担得起的药是各个国家一项非常重要的公共卫生事业。
新仿制药获批
患者可节约数百亿美元
根据美国FDA发布的一份题为《2018、2019和2020年度估计新仿制药批准带来的节约》报告显示,仿制药在2020年为患者节约了107亿美元,其中18亿美元来自首批仿制药批准贡献。2019年节约了248亿美元,其中94亿美元来自首批仿制药批准。2018年节约了178亿美元,其中40亿美元来自首批仿制药批准。这三年中,首批仿制药批准占总节约额的29%。
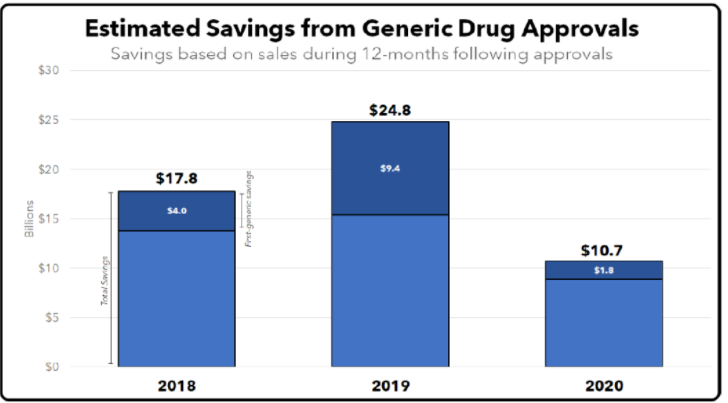
图片来源:参考资料1
另外,每年节约的变化主要是由于这些年批准的仿制药的产品组合。例如,当新的仿制药进入市场时,高价位、大市场的产品往往比小市场的产品产生更多的节约。例如,与2018年或2020年相比,2019年节余的大幅增加主要是由于少数高收入产品的批准。其中包括Viatris的神经和肌肉疼痛药物Lyrica的仿制药pregabalin,节省了66亿美元,约占2019年仿制药批准的所有仿制药节约的27%。在这些高收入产品获批较多的年份,新的仿制药获批的总节约可能明显高于高收入产品获批仿制药相对较少的年份。这些首个仿制药的批准时间往往由品牌产品的专利到期日决定。
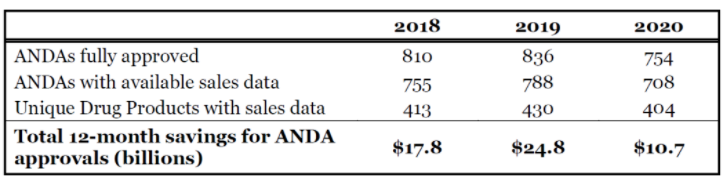
图片来源:参考资料1
除了总的节约,该报告还强调了与仿制药批准有关的价格下降的重要性。多数情况下,在首个仿制药批准后的一年内,价格比品牌价格下降了75%以上。比如,2012年5月,辉瑞的万艾可在韩国专利到期,第二天就有28个仿制药上市,价格仅为前者的三分之一,于是当月万艾可的销售额锐减了43%,市场价也被大大压低。而另外一些情况是对于其中一些服务于较小患者群体的产品来说,总的节约幅度不大。然而,对于依赖这些药物的病人来说,这些价格的降低是有意义的,可以增加他们获得重要药物的机会。
这些节约的贡献值有约20%来自印度。在FiercePharma发布的2021年全球仿制药巨头TOP10榜单,有4家公司来自印度。上世纪70年代,印度“铁娘子”英迪拉·甘地颁布了《专利法》:全球各地的药品,在印度不具有专利保护,本国公司可以随意仿制。于是印度开启了近20年的仿制药辉煌史,这期间大批印度药企涌现出来,为包括印度、欧美乃至全世界的病患带来廉价的仿制药。到现在,印度仿制药满足全球50%以上的各种疫苗需求,美国40%的仿制药需求以及英国25%的药品需求。
中国的仿制药市场几何?
既然FDA这份报告通过数据实打实给出了关于首批仿制药批准带来的节约。那么,我国的仿制药市场如何呢?从医药市场结构来看,目前我国制药企业中大部分也仍以仿制药为主。根据中国医药工业信息中心2021年8月发布的《中国仿制药蓝皮书》显示,2019年中国仿制药市场规模约为9707亿元,2020年仿制药整体市场规模受疫情影响跌至8087亿元。仿制药占比高达63%,而且仿制药的市场占比还在持续提升。从这个数据来看,我国的仿制药市场真的很“卷”。
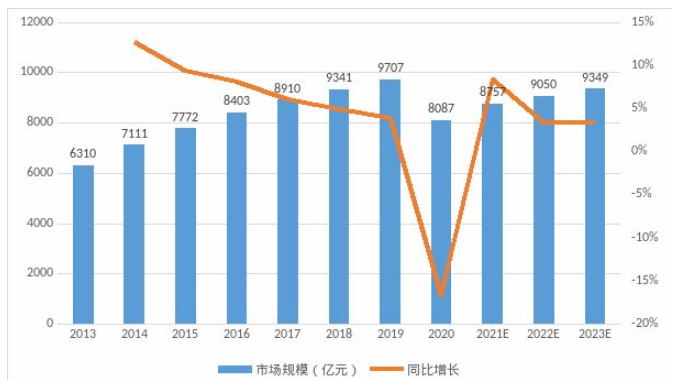
图片来源:参考资料2
这种状态来源于21世纪初,改革开放后,药厂经营许可权下放。一时间,药企数量从1320家猛增到世纪末的6357家。市场需求是有,但是又没啥研发能力,只好扎堆仿制,彼时的医药市场鱼目混珠,药品奇多。虚假繁荣之下,又缺乏有效的市场监管,价格也非常的混乱。以药养医丑闻层出不穷,生病本就已是一场灾祸,却还要扛起时代的灰。
于是医改应运而生:两票制/一票制政策、一致性评价政策以及集采政策。两票制/一票制政策压缩了中间的销售费用,用最高零售价限定利润空间,降低了药物流通成本。一致性评价政策则规避了摆烂式内卷的现状,通过强制仿制药与原研药进行再对比来提高仿制药质量。集采政策在一致性评价的基础上,又通过集中采购大幅度降低药品价格。
这么一套组合拳打下来,国内仿制药的暴利时代也一去不复返。同时,新的仿制药格局也因此重塑,仿制药的生产趋于商品化、标准化。
以药品批准日期计,2020年,仿制药一致性评价承办的受理号共计915个,通过的受理号数为591个。2021年,国产创新药获批数进入爆发期,仿制药获批数也大幅激增,NMPA共批准983个化药仿制药批文(含仿制3/4/6类),涉及品种达341个。根据国家药监局发布《关于发布仿制药参比制剂目录(第五十批)的通告》(2022年第2号)显示,2021年最受欢迎的仿制药TOP10按照企业数量排名分别为:他达拉非片、富马酸丙酚替诺福韦片、奥硝唑注射液、左氧氟沙星片、普瑞巴林胶囊、磷酸奥司他韦胶囊、利伐沙班片、非布司他片、吸入用盐酸氨溴索溶液、阿加曲班注射液。有趣的是,按照受理号数量排名,刚刚谈到的10种药品中有7种赫然在列。由此可见,曾经的热卖药在市场眼光看来依旧具有值得回味瓜分的市场。
小结
仿制药作为政府保障民有药所用,提高民众福祉的重要渠道,依旧具有广阔市场。而逐渐规范的市场,才是促进良性竞争的温床。无论什么时候,便宜好用的药总会有市场夹道欢迎。
参考资料:
1. FDA,《Estimating Cost Savings from New Generic Drug Approvals in 2018, 2019, and 2020》
2. 《中国仿制药蓝皮书》
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!