2020-08-17 11:58:24Source:药智网Views:402
第三批集采就要在8月20日开标,“集采入场券”一致性评价工作仍在有条不紊的进行中,截至8月14日,CDE受理一致性评价受理号累计2289个(592个企业的535个品种,按补充申请计,下同);其中已有661个受理号过评。本周(8月7日至8月14日),又有5个品种过评,多个超10亿级大品种在列;还有13个品种获承办...
过评详情
5个品种过评;10亿级「索拉非尼」首仿获批
本周有7个品规(5个品种)通过一致性评价,其中3个品种视同过评,2个为批准补充,且江西山香药业的甲苯磺酸索拉非尼片为国内首仿,具体详情如下:
本周一致性评价过评详情表
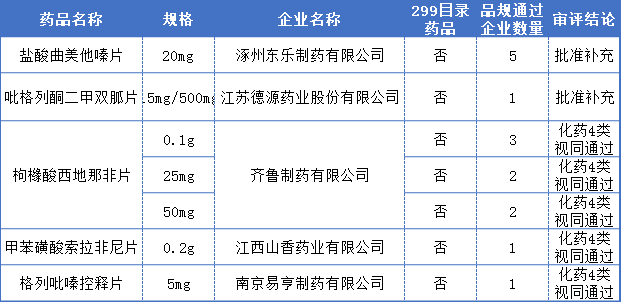
盐酸曲美他嗪片
盐酸曲美他嗪是第一个3-酮酰辅酶A硫解酶(3-KAT)抑制剂类代谢制剂,作为添加药物,用于对一线抗心绞痛治疗控制不佳或无法耐受的稳定型心绞痛成年患者的对症治疗。其原研企业为施维雅,最早在法国上市,2000年中国获批进口。
据药智数据,我国现有盐酸曲美他嗪片市场批文10条,包括原研企业在内,涉及生产厂家10家;2019年国内样本医院销售额为4.78亿元,其中超70%的份额为被原研企业占据,其次是瑞阳制药13.09%,本周过评的涿州东乐制药没有在销售TOP10之内。
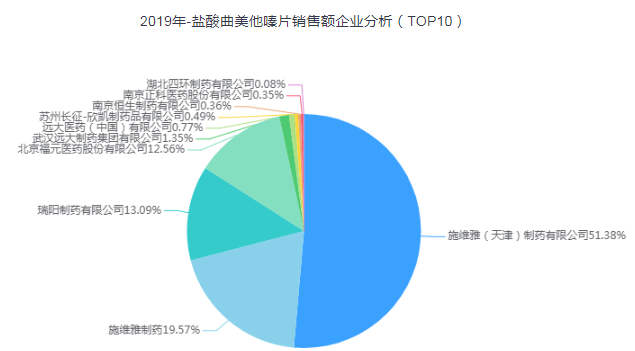
截至目前,盐酸曲美他嗪片累积已有5家通过一致性评价,分别是涿州东乐制药、瑞阳制药、远大医药、北京万生、江苏吴中、苏州制药厂。
吡格列酮二甲双胍片
吡格列酮二甲双胍片(复瑞彤)是吡格列酮和二甲双胍组成的复方制剂,用于治疗2型糖尿病。
据药智数据,我国现仅有江苏德源药业和杭州中美华东制药两家企业拥有该复方制剂市场批文;中国药学会样本医院数据(CPA数据)显示:2019年国内吡格列酮二甲双胍样本医院总体销售额约9016万元,江苏德源药业该产品样本市场占比6.79%;2020年一季度国内吡格列酮二甲双胍样本医院总体销售额约2279万元,江苏德源药业“复瑞彤”样本市场占比8.84%。样本市场销售额及占比均呈上升趋势。
另据药智网一致性评价进度数据库显示,江苏德源药业首家通过一致性评价,有望提升该药品的市场竞争力,为其将来销售增长奠定坚实的基础。
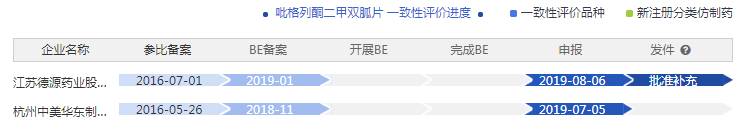
枸橼酸西地那非片
枸橼酸西地那非片为5型磷酸二酯酶(PDE-5)抑制剂,用于治疗罕见病成人肺动脉高压(PAH,WHO第1组),以改善运动能力和延缓临床恶化。西地那非的原研企业为辉瑞,FDA于1998年3月27日批准其上市,成为首个治疗ED的磷酸二酯酶-5(PDE-5)抑制剂为ED一线用药。
网络公开数据显示,2019年中国城市零售药店终端西地那非销售额超过23亿元,白云山市场份额占比第一,其次为原研企业辉瑞。
截止目前,枸橼酸西地那非片国产市场批文有13条,生产厂家7家,其中3个企业的3个品规已经通过一致性评价,本周齐鲁制药该品种按新化药4类注册获批,视同过评,向20亿级的抗ED市场发起挑战。
枸橼酸西地那非片一致性评价过评详情表

另值得提及的是枸橼酸西地那非片为第三批集采目录药品,齐鲁制药在即将开标之际,获批上市,来得早不如来得巧,正好搭上第三批集采的顺风车,形成3+1的竞标格局。
甲苯磺酸索拉非尼片
索拉非尼是一款口服多靶点、多激酶抑制剂。临床上主要用于治疗肝细胞癌、肾细胞癌和甲状腺癌。索拉非尼由拜耳研制,2005年12月获得FDA批准上市,2006年8月在中国获批,2017年通过国家谈判纳入医保乙类目录并在2019年再次降价成功续约。目前,国内医保支付标准为95元/片。
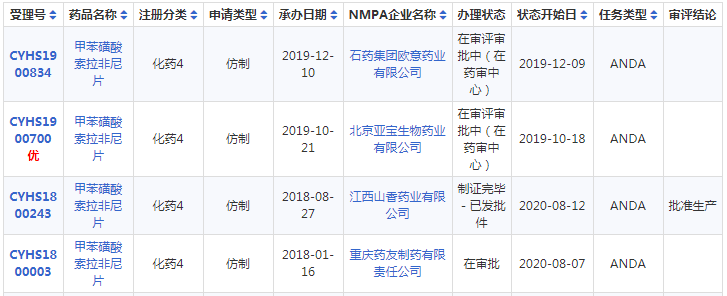
据悉,2019年,索拉非尼国内销售额约12亿元,其中样本医院销售额达6.6亿元,截止目前国内甲苯磺酸索拉非尼片仿制药申报上市的仅4家企业,山香药业一马当先,夺得首仿的同时视同通过一致性评价,打破原研壁垒。
甲苯磺酸索拉非尼片仿制药报产详情表
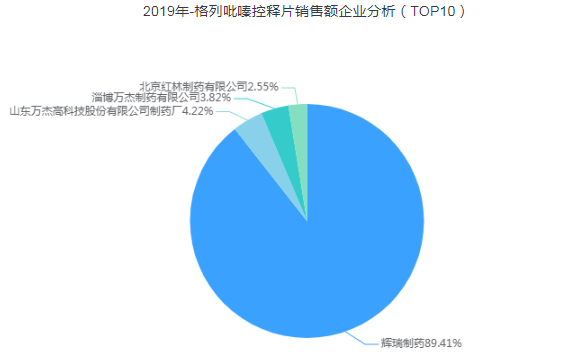
格列吡嗪控释片
格列吡嗪是一种磺脲类降糖药,由辉瑞开发;国内生产销售的剂型有片剂、分散片、口崩片、缓释片、控释片和胶囊剂等。据药智数据显示,其中控释片仅淄博万杰制药、北京红林制药、常州四药制药、以及刚获批的南京易亨制药4家国产企业获批生产。
2019年格列吡嗪控释片样本医院销售额为1.20亿元,其中原研辉瑞占据绝大部分份额,达89.41%。现除南京易亨制药首家视同通过一致性评价外,暂无其他企业过评,能否借此机会抢占原研份额,拭目以待。
申报受理
13个品种被承办,恒瑞核心首仿造影剂再获受理
本周CDE新增一致性评价受理号20个(13个品种),注射剂再次抢眼,有8个品种申报一致性评价被承办,恒瑞、倍特、石药中诺、罗欣等知名企业的重磅产品纷纷在列。
本周一致性评价申报受理详情
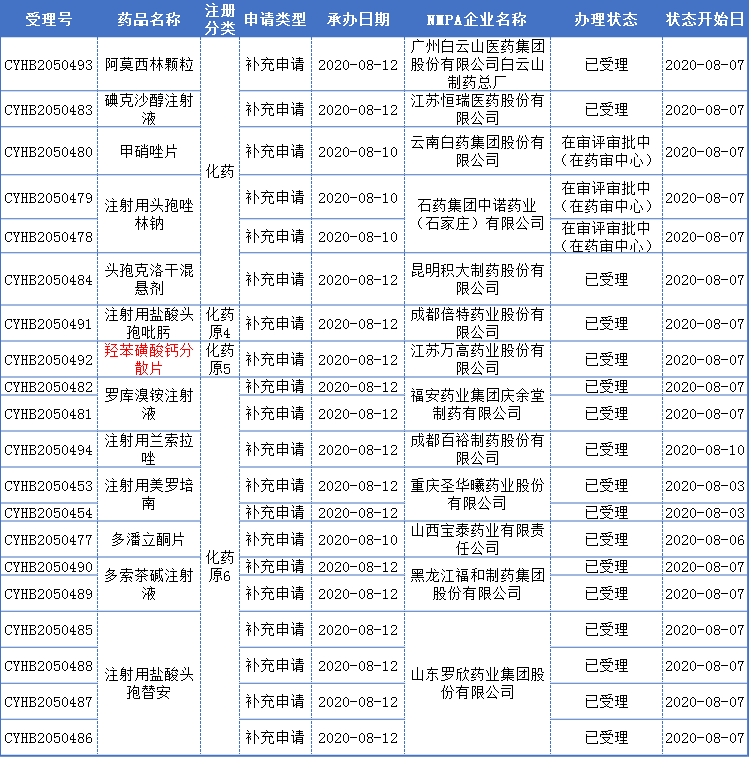
注:红的标注为本周首家申报受理品种
其中值得提及的是恒瑞医药的碘克沙醇注射液,碘克沙醇注射液是X-线对比剂,主要用于成人心血管造影、脑血管造影、外周动脉造影、腹部血管造影、尿路造影、静脉造影以及CT增强检查、儿童心血管造影。
恒瑞医药碘克沙醇注射液为国内首仿产品,且为恒瑞医药核心造影剂产品之一,中国医药工业信息中心的数据显示,2019年国内碘克沙醇市场规模为49.71亿元,占整个造影剂市场份额的35.65%。另据企业公告,2019年恒瑞造影剂实现营收32.3亿元,同比增长近39%,国内造影剂市占率排第一。
此前,恒瑞医药碘克沙醇注射液已有2个受理号申报一致性评价其中一个办理状态呈“已发件”状态,现又一受理号获受理,能否再次在首仿的基础之上抢先通过一致性评价,巩固首仿地位,获得更大造影剂市场蛋糕,可期可待。
碘克沙醇注射液一致性评价申报受理详情表

声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!