2020-08-20 09:11:57Source:毛三 贝壳社Views:754
近日,港交所官网信息显示,JW (Cayman) Therapeutics(以下简称:药明巨诺)已正式向港交所提交招股书,拟在香港主板上市。

作为国内细胞疗法“第一梯队”选手,药明巨诺早在2018年就拿下了国内首个以CD19为靶点的 CAR-T 产品 IND临床批件,到今年6月份,该产品的上市申请正式提交。实际上,自今年4月份开始,有关于“药明巨诺拟境外上市”的消息也开始在医药圈传开来。
如今尘埃落定。从招股书来看,药明巨诺此次赴港上市由高盛和UBS担任联席保荐人,拟IPO募资2-3亿美元,用于公司核心候选产品、其他候选产品、潜在管线产品以及营运资金和一般公司用途。
一旦赴港上市成功,药明巨诺将成为继南京传奇、永泰生物之后,国内第三家上市的CAR-T企业。
1
站在巨人的肩膀上
最新估值5.48亿美元
“药明巨诺成立的初衷,是想在中国建立起集研发、生产、销售为一体的细胞治疗公司平台。这个平台相对独立,不只是引进产品,也希望与其他海内外的公司合作引进创新的产品。”在去年年初接受E药经理人采访时,药明巨诺联合创始人兼CEO李怡平如是说。
时间拉回2016年。这一年4月,药明康德和美国 CAR-T 领域头部玩家Juno一拍即合,合资成立了药明巨诺,旨在聚焦CAR-T 和 TCR 疗法的研发和生产,开发用于血液瘤和实体瘤的细胞免疫疗法。
根据当时协议,药明康德和Juno分别持有药明巨诺50% 的股权。在Juno的在研产品达到开发里程碑后,药明巨诺有权选择产品在中国进行开发和销售,而Juno获取相应的预付款或股权、里程金以及产品上市后的销售提成。
Juno位于美国西雅图,作为全球CAR-T赛道的先驱企业之一,其手握重磅CAR-T研发管线,多个血液瘤和实体瘤的在研产品广泛覆盖CD19、CD22、BCMA、WT1等靶点。由于充分结合了Juno的国际顶尖技术优势,同时通过自主创新开发出更符合中国市场需求的生产工艺,药明巨诺在业内也被形容为是“站在巨人的肩膀上”。
虽头顶明星光环入场CAR-T赛道,药明巨诺在成立的头两年似乎颇为低调。直到2018年,药明巨诺以9000万美元融资再次高调出现在公众视野时,其显然已经迈入到一个全新的阶段,而那之后更是好消息不断:
可以看出,自2018年以来,药明巨诺可谓是一路开挂,不仅先后拿下系列融资,引入明星机构加持,同时核心产品也成功迈入商业化前夕的关键时刻,如今又将目光投向了港交所。
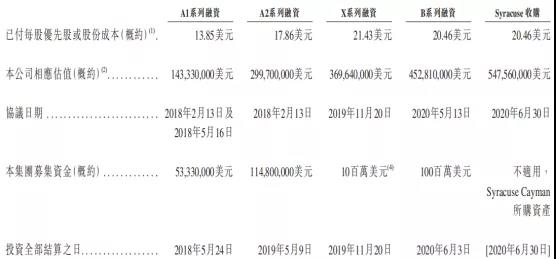
资料来源:招股书
从招股书来看,到2020年6月30日药明巨诺完成对Syracuse的收购之际,其估值已达5.48亿美元。
2
就差临门一脚
成立4年以来,药明巨诺建立了一个专注于血液癌症和实体瘤开发、制造和商业化突破性细胞免疫疗法的整合平台。
从招股书来看,目前药明巨诺已建立起全面且差异化的细胞免疫疗法产品管线,兼具已经验证有效的靶点及新型肿瘤抗原的候选产品,同时还设计了多个自体细胞疗法的细胞免疫疗法产品,涵盖血液癌症及实体瘤,具体情况如下:
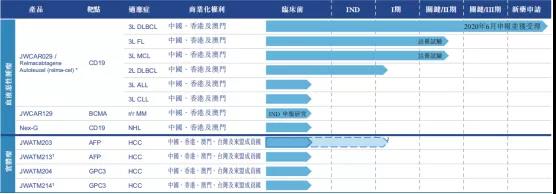
Relma-cel (JWCAR029)
Relma-cel是药明巨诺主打候选产品,靶向CD19 ,拟开发用于治疗复发或难治(「r/r」)B细胞淋巴瘤,有望成为中国首个获批的一类生物制品CAR-T疗法,并有望成为同类最佳CAR-T疗法。2020年6月,relma-cel的上市申请已经获得中国国家药监局(NMPA)受理,适应症为弥漫性大B细胞淋巴瘤的三线治疗。
据报道,Relma-cel在Juno公司 JCAR017基础上开发,其在中国的工艺优化过程便有商业化考虑。JCAR017原本在美国的工艺是将CD4和CD8细胞分离出来使用两条产品线生产,最后按照1:1比例混合回输到病人体内。而在中国,Relma-cel改良为提取CD4和CD8细胞后混合不做分离,在一条生产线上培养、生产后,再一起回输到病人体内。
招股书披露的临床数据显示,relma-cel在治疗经已接受大量预先治疗及预后不良的r/r DLBCL患者的注册临床试验中已证实其疗效,其中最佳ORR为75.9%,最佳CRR为48.3%。
JWCAR129
WCAR129以B细胞成熟抗原(BCMA)为靶点,是药明巨诺正在开发的一种自体CAR-T疗法,拟用于治疗多发性骨髓瘤(MM)。目前,该产品正在进行IND所需的临床前药理学、毒理学研究和制造流程开发研究,计划最早于2021年上半年开始临床研究。
下一代(「Nex-G」)抗CD19候选产品
药明巨诺在招股书中表示,其正在开发一套新技术和平台,以更短的生产周期时间,更高的质量,更好的产品特性以及更高的产品功效和安全性来支持下一代CAR-T产品和制造工艺,这将为其下一代抗CD19产品以及产品管线中的其他产品奠定基础。
JWATM203
JWATM203是临床前阶段及潜在同类首创以AFP为靶点治疗HCC的TCRmT细胞疗法,有潜质成为甲胎蛋白阳性HCC患者的绝佳治疗手段。目前,药明巨诺合作伙伴优瑞科已于美国推动其AFP TCRm T细胞疗法候选产品进行I/II期临床试验。通过与Lyell的合作,药明巨诺正在开发另一种以AFP为靶点治疗HCC的TCRm T细胞疗法JWATM213,或将进一步加强T细胞功能并提高疗效。
JWATM204
JWATM204是以GPC3为靶点的新型T细胞疗法候选产品,有潜质成为GPC3阳性HCC患者的绝佳治疗手段。与JWATM203及JWATM213相似,药明巨诺正利用Lyell技术开发另一种以GPC3为靶点的T细胞疗法候选产品JWATM214。
除了管线中的在研产品,药明巨诺在招股书中进一步表示,Juno管线中其他一些新产品未来也将继续扩充药明巨诺的研发管线。具体潜在产品如下:
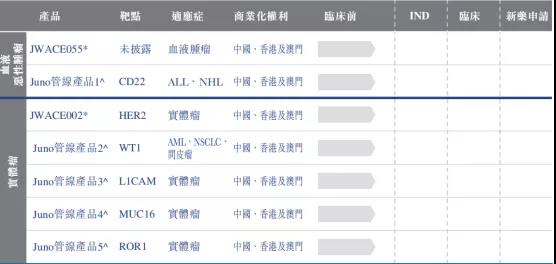
“药明巨诺未来发展过程将经历多个阶段。第一阶段是要通过合作、引进的方式在中国快速建立起来细胞治疗的平台,能够把美国Juno公司最好且成熟的技术和产品尽快引进到中国。”在去年年初接受E药经理人的采访中,李怡平在谈到药明巨诺未来的发展规划时如此表示。
当下来看,在“将Juno成熟的技术和产品尽快引进到中国”这件事上,药明巨诺似乎只差临门一脚。
3
上市潮&商业化:
火热的CAR-T市场
实际上,在药明巨诺提交JWCAR029上市申请的4个月前,复星凯特已抢先一步提交了其首个CAR-T药物FKC876的上市申请,成为中国首个申报上市的CAR-T细胞疗法。
而除了药明巨诺和复星凯特,目前还有两款CAR-T产品处于上市申请阶段,一是BMS/蓝鸟的ide-cel(bb2121)、二是BMS的liso-cel(JCAR017)。此外传奇生物CAR-T产品LCAR-B38M 也计划将于2020年下半年提交上市申请。
可以说,进入2020年以来,CAR-T细胞疗法已迎来产品上市倒计时的关键阶段,商业化大幕拉开在即。而在国内,伴随着即将到来的产品商业化,CAR-T药企们也纷纷将目光锁定资本市场。今年以来,除了刚刚递交赴港上市申请的药明巨诺,此前传奇生物、永泰生物已成功登陆纳斯达克和港交所,开启资本新征程。
回到商业化问题上,尽管当下包括药明巨诺在内的数家CAR-T药企已陆续提交新药上市申请,竞争氛围似乎已颇为激烈。但由于CAR-T疗法仍处于开发早期阶段,市场可谓依旧是蓝海一片。
根据药明巨诺招股书数据,全球CAR-T市场由2017年的约1.3亿美元增至2019年的约7.34亿美元,预期于2024年将进一步增长至47亿美元,于2023年增长至181亿美元。中国CAR-T市场预期将于2024年增长至人民币54亿元,并于2030年增长至人民币243亿元。2024年至2030年的复合年增长率为28.7%。
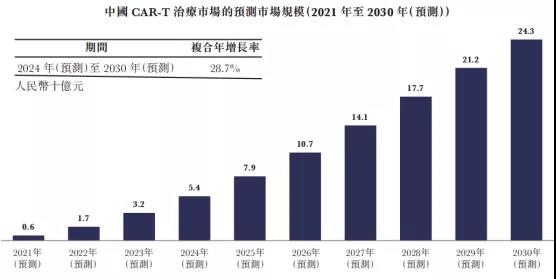
资料来源:招股书
不过在CAR-T这一赛道,如果从第一梯队往后看,的确颇为拥挤。公开数据显示,至2019年5月30日,全球范围内共有1011项细胞治疗在研产品的研究,其中美国有439项,中国有305项,中美两国占比达到全球细胞疗法的73.59%,其中CAR-T的研发项目数高达568项。
从靶点来看,目前 Car-T 细胞治疗的临床试验主要集中在 CD19,CD20,CD22, BCMA等靶点。此前,在前不久,《Nature Reviews Drug Discovery》杂志就对全球细胞疗法进行深度盘点表示,CD19位列最受欢迎的TOP10靶点之首,已连续多年蝉联血液瘤适应症最主要的靶点。目前全球仅获批的诺华和吉利德两款CAR-T疗法也正是靶向CD19,在国内,靶向CD19的CAR-T还包括以下企业:
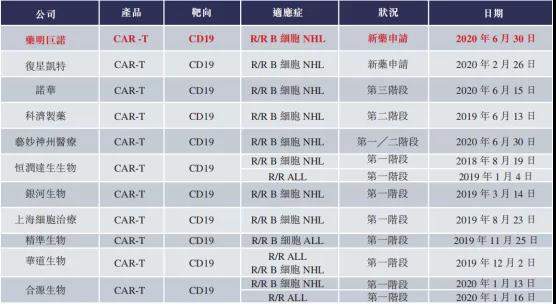
资料来源:招股书
另一个热门靶点是BCMA,目前国内布局BCMA的CAR-T药企主要包括传奇生物、科济生物、恒润达生等,其中以传奇生物进度最为领先。6月5日,传奇生物正式登录美国纳斯达克,上市首日股价上涨60.8%,总市值飙升至近50亿美元,成为国内CAR-T第一股。
从估值来看,传奇生物IPO之前估值约20亿美元,药明巨诺目前估值5.4亿美元,虽与传奇生物存在一定差距,但作为国内第三家上市的CAR-T企业,仍值得期待。
声明:本文系药方舟转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!