

江苏宜明生物科技有限公司(简称“宜明生物”),成立于2015年,是一家致力于先进治疗药品(ATMP) 技术的开发和应用、提供一站式CDMO整体解决方案、全球化布局的企业。
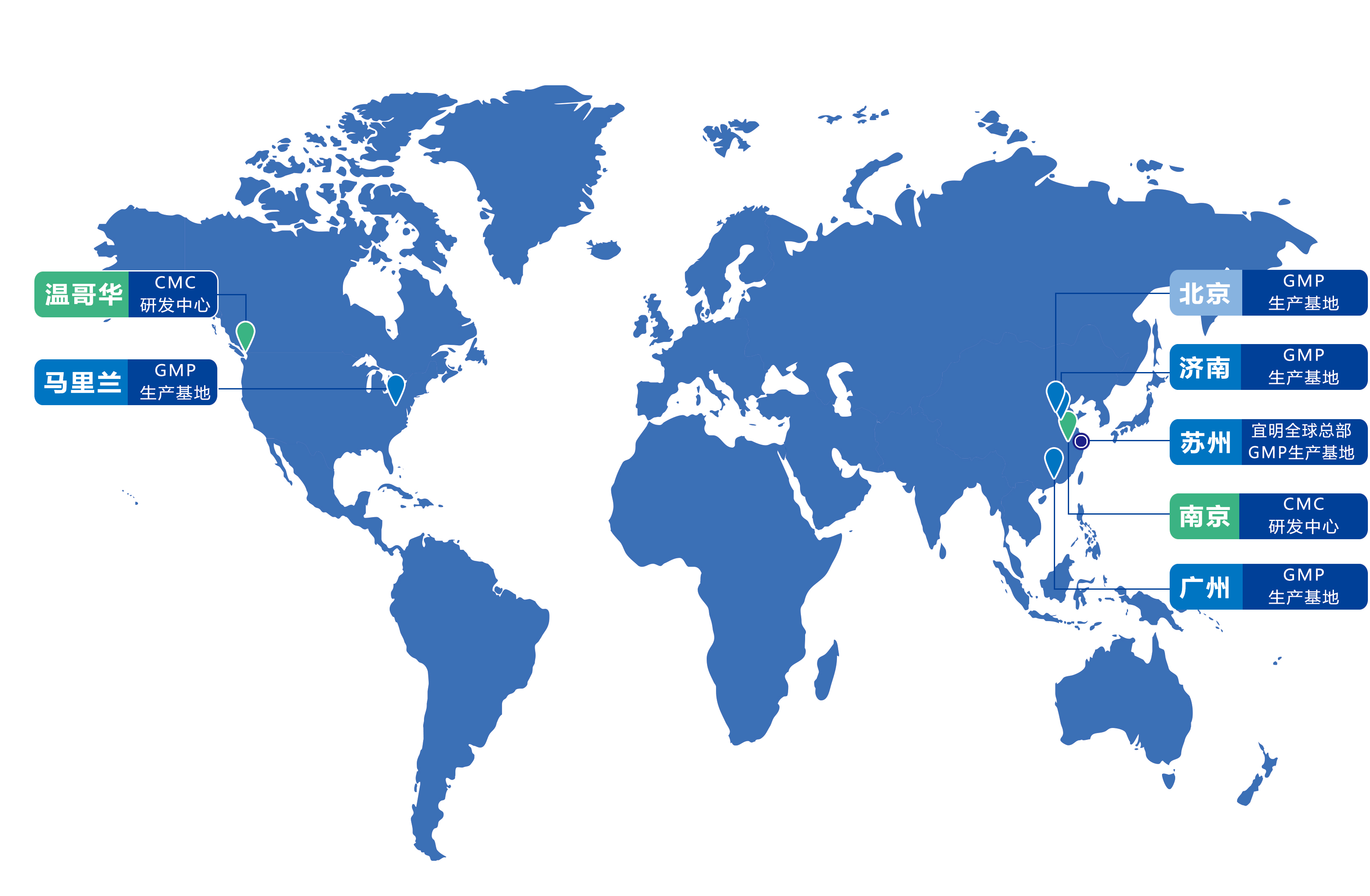
宜明生物在马里兰、苏州、济南、广州、北京建立GMP 生产基地,已启用生产场地近20000平米,在全球拥有约五十条GMP生产线,并在温哥华、南京设立了专注于前瞻性技术开发应用的全球研发中心。依托经验丰富的国际化专家团队和中美两地GMP生产基地,宜明生物能够为全球ATMP企业提供从早期研发到商业化生产的全流程工艺开发与生产制备等服务。
目前,宜明生物已承接/交付IIT、IND、临床Ⅰ/Ⅱ期产品百余批次,帮助全球ATMP企业完成多项创新药物IND获批临床,其产品涵盖免疫细胞药物、干细胞药物、基因药物、核酸药物、溶瘤病毒药物、基因编辑元件sgRNA等。
CDMO服务:宜明生物是一个前瞻性、规模化的细胞及基因治疗公共服务平台,从厂房设计到生产运营符合GMP生物制品规范要求。依托经验丰富的国际化专家团队和全球GMP生产服务网络,宜明生物能够为全球CGT企业提供从早期研发到商业化生产的全流程工艺开发和生产交付服务以及进入全球市场的注册申报服务。
CRO服务:依托全球的前瞻技术研发中心的技术创新和成熟的CDMO生产工艺平台,宜明生物能够为全球客户提供CGT领域基础研究和临床前研究的CRO服务,CRO服务涵盖DNA、RNA、病毒、蛋白,检测等。
分析检测服务:宜明生物的专有分析平台配备了先进的分析仪器,包括AUC、HPLC、qPCR、ddPCR、CE 和流式细胞仪等。凭借一流的自主一站式分析与检测平台以及专业的技术团队,宜明生物建立了涵盖生物化学(包括分子、生物细胞及蛋白质)、物理化学、微生物学三大检测平台,确保CGT产品的安全和标准化。我们的服务包括通过不同的表征方法测定CGT产品的物理特性、识别、滴度/含量、纯度和安全性等。能够开发基于不同产品理化性质的质量控制方法,为不同类型的产品提供定制化服务。
现货产品供应:依托成熟稳定的CGT CDMO生产工艺,宜明生物能够为CGT领域研究人员提供符合科研级和GMP级现货产品,助力先进治疗药品(ATMP)的研发进度与商业化生产。
GMP 质粒
宜明生物搭建Ubri-Perfect TM GMP 质粒生产平台,专注于临床级GMP质粒的大规模生产工艺开发,拥有完善的平台化生产工艺以及质量管理体系,可为客户提供从临床前到商业化阶段的环状质粒和线性化质粒一站式服务。
GMP 腺相关病毒(AAV)
腺相关病毒(AAV)具备安全性高、免疫原性低、高效持续表达和易于操作等优点,是基因治疗领域备受瞩目的病毒载体。然而AAV生产过程复杂 ,其中放量生产以及产能等一直是AAV商业化生产的主要瓶颈。宜明生物致力于病毒载体的研发与制备,其 Ubri-AdvancedTMGMP AAV生产平台工艺可扩展,可实现50L-200L-500L-2000L商业化生产规模、具备成本效益、可提供覆盖全生产流程的解决方案。
GMP 慢病毒
慢病毒载体(Lentivirus,LV)是细胞与基因治疗中应用最为广泛的载体之一,其产能和成本控制是慢病毒载体制造面临的主要挑战。宜明生物Ubri-leaderTM GMP慢病毒生产平台整合了高效的质粒生产平台、专有的无血清悬浮细胞培养平台以及慢病毒制备平台,可实现小-中-大规模生产、具备成本效益、可提供覆盖全生产流程的解决方案。
GMP 溶瘤病毒
溶瘤病毒( OVs)是一类具有复制能力的肿瘤杀伤型病毒的总称,主要包括 Adenovirus,Vaccinia virus,Herpes Simplex Virus等。溶瘤病毒具备特异杀伤肿瘤细胞的能力,直接杀伤肿瘤细胞的同时可增强受感染肿瘤细胞对细胞因子等引起的免疫反应的敏感性,加速受感染细胞的裂解。
宜明生物致力于病毒载体的研发与制备,其病毒载体生产平台工艺可扩展,可实现50L-200L-500L-2000L商业化生产规模、具备成本效益、可提供覆盖全生产流程的解决方案。
GMP mRNA-LNP
随着基于脂质纳米颗粒(LNP)的COVID-19 mRNA疫苗的成功,通过LNP输送的RNA治疗药物的潜力已受到广泛关注。相比需要大规模培养真核细胞的病毒载体,非病毒传递载体(如mRNA-LNP)的生产更为简单。宜明生物建立完善的Ubri-MarsTM RNA制备平台,采用体外转录(IVT)平台制备mRNA,结合微流控技术进行LNP封装,为客户可提供GMP 级别的mRNA LNP 一站式CDMO服务。
GMP sgRNA IVT
在基因编辑中,Cas蛋白和gRNA的形成复合物,由gRNA的特异序列指引与基因组特意靶点结合,并造成该位点的DNA双链断裂,逐渐成为CRISPR/Cas9技术更高效的实现途径。宜明生物采用体外转录(IVT)工艺,避免大规模化学合成gRNA成本过高,及有毒化学试剂残留风险的问题,通过添加3’端Aptamer特殊序列提高了细胞内gRNA的稳定性。为您在细胞与基因治疗领域的研究提供高质量的sgRNA一站式CRO和CDMO整体解决方案。
GMP iPSC
iPSC的发现为医学界带来了新的视角和福音,而通过iPSC技术与CRISPR/Cas9基因编辑技术联用,可以实现个性化治疗,更是开启了疾病治疗的新篇章。宜明生物开发并建立完善的Ubri-PsycheTM iPSC重编程工艺平台,并可提供GMP级别的基因编辑元件生产(cas9/mRNA、dsDNA、sgRNA)以及iPSC细胞建库一站式服务。专有的创新技术在显著提高元件稳定性的同时,其简化的制备工艺还可大幅度降低商业化生产成本,让创新成果惠及更多患者。
GMP CAR-T
细胞治疗在治疗某些恶性肿瘤方面取得了显著成效,如同向人体内引入了一支具有特殊装备的军队,特异性靶向杀伤肿瘤细胞。宜明生物创新性的自动化、全封闭Ubri Cure TM GMP 细胞治疗平台,可为 CAR-T细胞治疗产品提供工艺开发及放大、分析方法开发与质量研究、临床样品生产与放行、中美欧 IND 申报等一站式CDMO 服务模式。
菌种库构建
稳定良好的菌种库系统的建立是保证生产工艺一致性的至关重要的一环。宜明生物GMP厂房设有专门的原核细胞库构建车间和单独的储备车间,可提供原始种子库(PCB)、主种子库(MCB)和工作种子库(WCB)的构建以及储存服务,提供完整的符合现场核查的GMP资料。所有菌种库均按照NMPA及FDA要求进行鉴定验证,确保纯度和稳定性。
细胞库构建
稳定良好的细胞库系统是保证生产工艺一致性的重要一环。宜明生物GMP厂房设有专门的真核细胞库构建和储备车间,可提供原始细胞库(PCB)、主细胞库(MCB)和工作细胞库(WCB)构建以及储存服务。宜明生物专有的悬浮293XS和贴壁293T、悬浮293TH细胞株适用于AAV和慢病毒的规模化工业生产。所有细胞库均按照NMPA及FDA要求进行鉴定验证,确保纯度和稳定性。
全球注册申报服务
宜明生物在中美两地均拥有经验丰富的注册团队,能够为ATMP产品开发的整个生命周期中提供注册申报服务,从pre-IND到BLA以及DMF备案,覆盖美国、加拿大、中国、欧盟、澳大利亚在内的各国和地区。
| Job Title | City | Working Experience | Education background | Pubdate | Salary | |
|---|---|---|---|---|---|---|
| Loading... | ||||||

You can input 200 words